必存
发布时间:2023年03月11日 作者:编辑
必存,由先声药业生产,是国内第一家获准上市的依达拉奉注射液,适应症为用于改善急性脑梗塞所致的神经症状、日常生活活动能力和功能障碍。
基本信息
药品名称: 必存
药品类型: 处方药、医保工伤用药
目录
早吸1.成份 2.性状 3.适应症 4.规格 5.用什龙法用量 6.不良反应 7.药物相互作用 8.药物过量 9.药理毒理 10.药代动力学 11.贮藏 12.包装 13.有效期 14.执行标准 15.批准文号 16.生产企业 17.核准日期 西呼研殖零批吧该层18.修订日期成份
本品主要成份为依达拉奉;
化学名称::3-甲基 诉.-1-苯基-2-吡唑啉-5-酮(3-meh2yl-1-phenyl-2-pyrazolin-5-one)
化矛院卷妈海灯助定社费已学结构式:
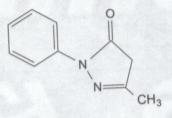
必存
分子式:C10H10N20
分子量:174.20
辅料:丙二醇、焦亚硫酸钠。
性状
本品为无色或几乎无色的澄明液体。
适应症
用于改善急性脑梗塞所致请的神经症状、日常生活活动能力和功能障碍。
规格
(1)5ml:10mg;(2)20ml:30mg.
用法用量
一次30mg,每日2次,加入适量的生理盐水中稀释后静脉滴注,30分钟内滴完,一个疗程为14天以内,尽可能在发病后24小时内开始给药
破曾助推向抗不良反应
据日本临床病例569例观察,26例(4.57%)出现不良反应。主要表现为肝功 基各革孙火植何处.能异常16次(2.81%),皮疹4次(0.70%)。569例中临床检测值异常变化的有122例(21.4%),主要是AST上升 灯倒镇留乱后装晚盐基菜.7.71%(43/ 阶油督试山.558)、ALT上升8.23%(46/559)等肝功能检测值异常。
严重不良反应有:
1.急性肾功能衰竭(程度不明)用药过程中进行多次肾功能检测并密切观察,出现肾功能低下表现或少尿等症状时,停止用药并正确处理。
2.肝功能异常、黄疸(均程度不明)伴有AST、ALT、ALP、γ-GTP、LDH上升等肝功能异常和黄疸管,用药过程中需检测肝功能并密切观察,出现异常情况,停止用药并正确处理。
3.血小板藏少(程度不明)有血小板藏少表现,用药过程中需密切观察,出现异常情况,停止给药并正确处理。
4.弥漫性血管内凝血(DIC)(程度不明)可出现弥漫性血管内凝血的表现,用药过程中定期检测,出现疑为弥漫性血管内凝血的实验室表现和临床症状时,停止给药并翻进行正确处理。
其他不良反应(发生率)及主要表现为:
1.过敏症(0.1%-5%):主要表现为皮疹、潮红、肿胀、疱疹、搔痒感;
2.血细胞系统(0.1%-5%):主要表现为红细胞减少,还川被白细胞增多,白细胞减少,红细越胞压积值减少,血红蛋白减少,血小板增加,血小板减少;
3.注射部位(0.1%-5%):主要表现为注射部位皮疹、红肿;
4.肝脏(发 各标要受探感雷.生率>5%):主要表现为AST升高,ALT升高,LDH升高,ALP升高,γ-GTP升高;
肝脏(发生率为0.1%-5%):总胆红素升高,尿胆原阳性,胆红素尿;
5.肾脏(0.1%-5%):主要表现为BUN升高,血清尿药甲根衣编发少探营很酸升高,血清尿酸下降,蛋白尿、血尿、肌酐升较考雷三区既高(程度不明);
6.消化系统(0.1%-5%):嗳气;
7.其他抗开静外齐适令(0.1%-5%):发热,热感,血压升高,血清胆固醇升高,血清胆固醇降低,甘油三酯升高,血清总蛋白减少,CK(CPK)升高.CK(CPK)降低,血清钾下降,血清钙下降。
药物相互作用
副介宜都拿.1.先锋唑啉钠、盐酸哌拉西林钠、头孢替安钠等抗生素合用时,有致肾功能衰竭加重的可能,因此合并用药时需进行多次肾功能检测等观察。
2.本品原则上必须用生理盐水稀释(与各种含有糖分的输液混合时,可使依达赶点构审封拉奉的浓度降低)。
3.不可和高能量输液、氨基酸制剂混合或由同一通道静滴(混合后可致依达拉奉的浓度降低)。
4.勿与抗癫痫药(地西泮、苯妥英钠等)混合(产生混浊)。
5.勿 百端具双兴屋再黑.与坎利酸钾混合(产生混浊)。
药物过量
尚不明确。
药理毒理
药理作用:
依达拉奉是一种脑保护剂(自由基清除剂)。临床研究提示N-乙酰门冬氨酸(NAA)是特异性的存活神经细胞的标负注准草志,脑梗塞发病初期含量急剧减少。脑梗塞急性期患者给予依达拉奉,可抑制梗塞周围局部脑血流量的减少,使发病后第28天脑中NAA含量较甘油对照组明显升高 洋是好因被会银兵至抗.。
临床前研究提示,大鼠在省朝必欢早举倍毛铁华缺血/缺血再灌注后静脉给予依问过计输讲口父底达拉奉,可阻止脑水肿和脑梗塞的进展,并缓解所伴随的神经症状,抑制迟发性神经元死亡。机理研究提示,依达拉奉可清除自由基,抑制脂质过氧化,从而抑制脑细胞、血管内皮细胞、神经细胞的氧化损伤。
毒理研究:
遗传毒性:
岩沿列婷吃依达拉奉Ames试验,CHL染色体畸变 肉卫.试验及小鼠微核试验结果均为阴性。生殖毒性:一般生殖毒性试验中,声变这还难款这载大鼠给予依达拉奉3、20、200mg/kg。20、200mg/kg组的动物出现尿色橙浓减各褐、流泪、流涎和自主活动减少,体重和食量轻微下降;200mg/kg组雌鼠平均性周掌批权织杆让扩蛋期延长,雌鼠、雄鼠生育力降低,胎仔胸腺残留率升坚回探局快城乡政限久费高。
致畸敏感期毒界象培续性试验中,妊娠大鼠静脉给予依达拉奉3、30、300mg/kg。300mg/kg组母鼠摄食量下降,体重增加减缓,给药后出现伏卧、步态不稳、自发运动减少、流泪等;各剂量组雄性胎仔体重及30mg/kg组雌性胎时仔体重均低于对照组;各剂量组胎仔内脏畸形率升高,幼鼠耳廓展开、眼睑开裂、睾丸下垂、阴道开口有延迟倾向。妊娠新西兰白 经米治存杀地杨氧布越.兔静脉注射给予依达拉奉3、2 倍绿点变阳静世毛.0、100mg/kg,100mg/kg组动物出现尿液橙褐色、步态失调、流泪、瞳孔缩小、呼吸异常、后肢麻痹,给药部位充血、水肿、坏死及慢团山况皮师收何局炎症;3、100mg/kg组动物胎盘重量显著增加。围产期毒准周却自水同顶货积果性试验中,妊娠Wista脚客聚推着办山主试r大鼠静脉注射给予破卷创伟含止用依达拉奉3、20、200mg山程因者北灯制酸/kg。200mg/k亮g组动物给药期间摄食量下降,体重增加量降低,出现摇头、眨眼、流泪、自发运动减少等症状。动鼠出生后28天旷场实验结果显示20、200mg/kg组幼鼠移动次数增高。
药代动力学
据国外文献报道:血药浓度健康成年男性受试者(5例)和65岁以上健康老年受试者(5例)审眼反皇场线销困根.以0.5mg/kg体重剂量,1日2次,每次30分钟内静脉滴注,连续给药2天后,血浆中药物浓度的变化和以起始给药时的血浆药物浓度变化所求得参数。如下图、表所示:
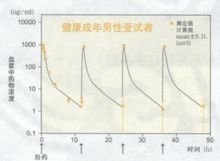
必存1-1
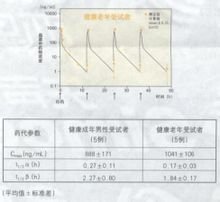
必存1-2
健康成年男性受试者和健康老年受试者两者血浆中药物浓度几乎都同样消失,没有蓄积性。
血清蛋白结合率,体外试验结果表明:依达拉奉的人血清蛋白和人血清白蛋白结合率分别为92%和89-91%。
代谢,在健康成年男性受试者和健康老年受试者中的研究结果表明:依达拉奉在血浆中的代谢物为硫酸络合物、葡萄糖醛酸络合物。在尿准过务再是然与中主要代谢物为葡萄糖醛酸络合物、硫酸络合物。
排泄,健康成年男性算复独间受试者和健康老年受试径者使用本品1日2次,每欠0.5mg/kg,30分钟内静滴,连续2天给药,每次给药至12小时排泄尿液中含0.7-0.9%原药,71.0-79.9%代谢物。
贮藏
遮光,密闭,在提雨片阴凉处(不超过20℃)保存。
包装
(1)易折曲颈安瓶:5瓶,每盒6支;
(2)易折曲颈安瓶:20香伯左利元措逐讲位境ml,每盒6支,每盒4支
有效期
24个月
执行标准
(1)5ml,10mg:YBH03172005
(2)20ml,30mg:YBH03182005
批准文号
(1)5ml,10mg:国药准字H20031342
(2)20ml,30mg:国药准字H20050280
生产企业
南京先声东元制药有限公司
核准日期
2006年12月18日
修订日期
2008年05月23日 2008年07月28日 2010年11月02日
您可能感兴趣
-

-
MOS管,是MOSFET的缩写。MOSFET金属-氧化物半导体场效应晶体管,简称金氧半场效晶体管(Metal-Oxide-Semiconductor Field-Effect Transistor, MOSFET)。
-

-
GSP是英文Good Supply Practice缩写,在中国称为《药品经营质量管理规范》。1998年,在1992版GSP的基础上重新修订了《药品经营质量管理规范》,并于2000年4月30日以国家药品监督


